-
 企业端
企业端
 企业端
企业端
-
 医院端
医院端
 医院端
医院端
-
 系统概述
系统概述
-
 UDI政策
UDI政策
-
 企业介绍
企业介绍
UDI云平台(系统介绍)
UDI云平台是中国二维码注册认证中心的UDI云应用系统,为客户提供安全易用的UDI全面应用服务,涵盖ISO发码、UDI标识与载体质量检测、产品资料、DI、PI数据管理、一维码、二维码标签印制等扩展服务。
本平台基于中国国家药品监督管理局《医疗器械唯一标识系统规则》(简称“UDI系统”)建立的系统体系。医疗器械注册证持有人(含医疗器械生产企业)落实UDI系统需要建设三个重要目标:产品标识载体的选择与赋码、企业自有UDI数据库建设、上传DI数据至国药监UDI数据库。
本系统的产品管理模块,提供产品信息以及其对应的DI信息的录入、存储功能,为标识载体的产品赋码提供了必要准备。
本系统的标签打印模块,提供产品赋码实施的落实功能。通过标签模版设计,建立标签模板,关联产品信息;通过批量套打的过程功能,自动生成UDI标识并完成数据库录入,企业仅需通过自动设备或人工完成赋码动作即可。
本系统的数据预审和上传模块,为付费用户提供产品DI数据的预审和国药监UDI数据库上传功能。用户通过选择需要预审的DI数据条目,本系统将生成该笔数据的预审上传单,后台合规人员对数据进行合规预审。通过预审后,经由企业许可,本系统24小时内自动上传至国药监UDI数据库。
本系统还提供基于UDI扩展的各种便捷实用功能,如企业发码、标签质量检测、各模块的批量工具等多种小功能,保证用户在使用过程中的最佳体验。
UDI政策简介
2015年5月,习近平总书记在主持中共中央政治局第二十三次集体学习时强调,要切实加强食品药品监管,用最严谨的标准、最严格的监管、最严厉的处罚、最严肃的问责,加快建立科学完善的食品药品安全治理体系,坚持严管并重,严把从农田到餐桌,从实验室到医院的每一道防线。
2019年07月03日,国家药监局 国家卫生健康委《医疗器械唯一标识系统试点工作方案》(药监综械注〔2019〕56号) (一)2019年7月,确定试点品种、参与单位。成立唯一标识系统试点工作部门协作工作小组,印发试点工作方案。组织开展试点培训,启动试点工作。试点单位制定实施方案,细化任务措施,明确验收指标。(二)2019年8月—11月,组织验证医疗器械唯一标识的创建和赋予。(三)2019年12月—2020年2月,组织验证医疗器械唯一标识数据库的上传、下载和接口标准。(四)2020年3月—6月,组织验证唯一标识数据的部门间衔接和扩展应用。(五)2020年7月,组织召开试点总结会,形成试点报告,完善首批产品唯一标识实施方案。
2019年7月3日,国家药监局 国家卫生健康委《医疗器械唯一标识系统试点工作方案》(药监综械注〔2019〕56号) (一)2019年7月,确定试点品种、参与单位。成立唯一标识系统试点工作部门协作工作小组,印发试点工作方案。组织开展试点培训,启动试点工作。试点单位制定实施方案,细化任务措施,明确验收指标。(二)2019年8月—11月,组织验证医疗器械唯一标识的创建和赋予。(三)2019年12月—2020年2月,组织验证医疗器械唯一标识数据库的上传、下载和接口标准。(四)2020年3月—6月,组织验证唯一标识数据的部门间衔接和扩展应用。(五)2020年7月,组织召开试点总结会,形成试点报告,完善首批产品唯一标识实施方案。 2019年8月23日,国家药监局关于发布医疗器械唯一标识系统规则的公告,《医疗器械唯一标识系统规则》自2019年10月1日起施行(2019年 第66号) 2019年8月27日,国家药监局综合司 国家卫生健康委办公厅 关于成立医疗器械唯一标识系统试点工作部门协作工作小组的通知(药监综械注〔2019〕76号) 2019年9月1日起,北京市卫健委:北京市各级医疗机构将动态监测医用耗材,植入性医用耗材必须记入患者病历。 2019年10月15日,国家药监局关于做好第一批实施医疗器械唯一标识工作有关事项的通告(2019年第72号)针对列入第一批实施产品目录的医疗器械: 2020年10月1日起,生产的医疗器械应当具有医疗器械唯一标识; 2020年10月1日起,生产的医疗器械在其上市销售前,注册人应当按照相关标准或者规范要求将最小销售单元、更高级别包装的产品标识和相关数据上传至医疗器械唯一标识数据库;
UDI云平台-独立的第三方大数据平台
- 中国二维码认证与管理中心授权的代码发行机构(ISO、CEN、AIM联合认可)。
- 中国互联网药品信息服务提供商。
- 中国首批【医疗器械网络交易服务第三方平台】。
- “UDI云”知识产权所有者。
UDI云平台是国家药品监督管理局指定UDI发码机构中关村工信二维码技术研究院(ZIIOT)授权的独立代码发行机构(授权证书请见附录),可按照医疗器械唯一标识MA(IDcode)编码规则为医疗器械注册人和备案人提供医疗器械唯一标识相关的一体化解决方案,包括但不限于UDI发码和赋码、标签检测与验证、UDI系统的建立和维护、软硬件采购及与UDI系统的集成等服务。
UDI云平台具有“UDI云”软件著作权,为客户提供云托管、云解析服务,并可进行私有化部署与定制。
UDI云平台可为客户提供按照ISO 15415和ISO 15416进行的UDI标识与载体质量检测服务。
UDI云平台案例
医疗产品一械一标、一物一码结合“UDI云平台”,助力客户研发、注册、生产、流通、使用、退市全程合规。

- 意大利进口BLB产品UDI案例
- 某中德合资医疗器械UDI案例
- 某香港上市医疗器械UDI案例
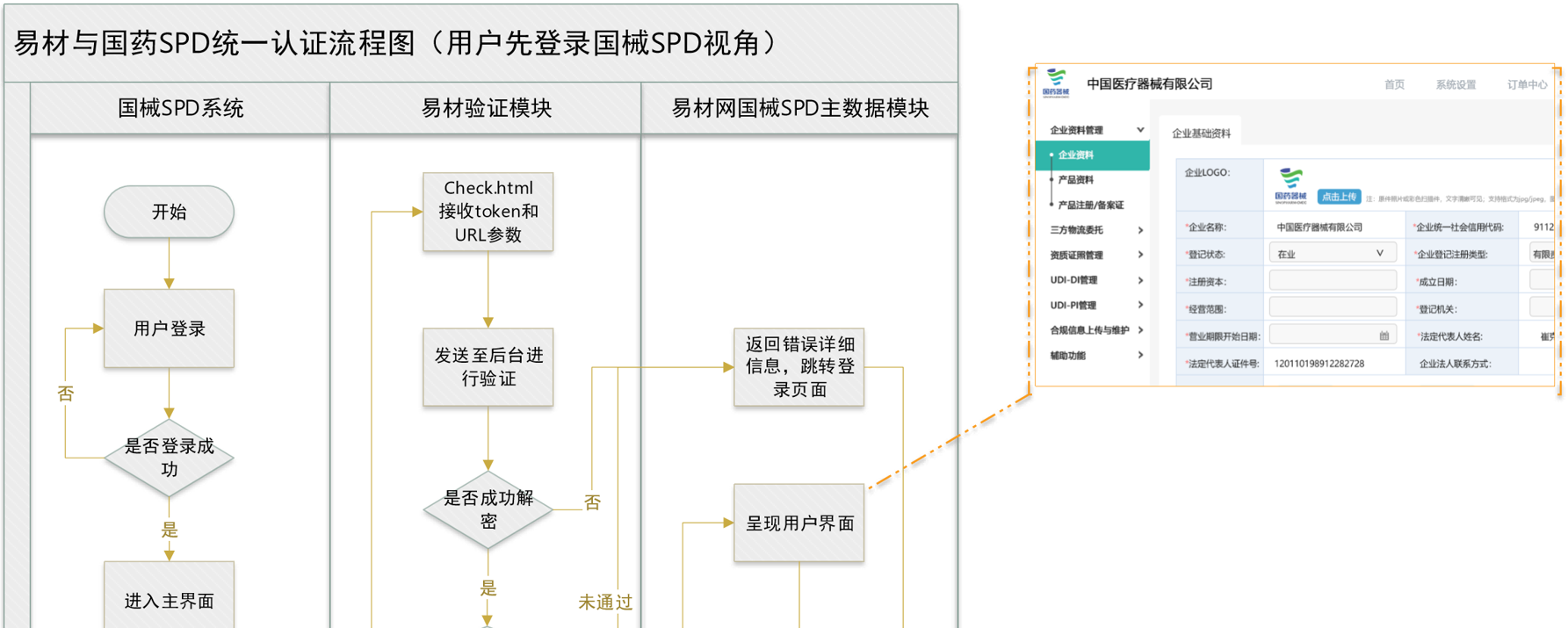
- 某香港上市医疗器械UDI案例
-

- 微信服务号:物码服务
-

- 微信订阅号:物码中心